CANCER DE PROSTATA
NUEVO PARADIGMA DIAGNOSTICO TERAPEUTICO
INTRODUCCION
El Adenocarcinoma de Próstata es una patología de gran presencia dentro de la práctica clínica habitual fundamentalmente debido al uso extendido del Antígeno prostático Específico para la detección del Cáncer de Próstata, por que es una patología prevalente dentro de los adultos mayores que son una subpoblación importante dentro del medio hospitalario y de la demanda de la medicina de atención primaria. Además algunas de sus complicaciones, ya sea secundario a su evolución natural o al tratamiento Uro – Oncológico impuesto, pueden suponer el compromiso de otras áreas clínicas.
Aún así, siendo una entidad nosológica, por ende, bastante conocida y estudiada, persisten dudas respecto a lo que es la Interpretación del PSA del Screening del Cáncer de Próstata, y dentro del estudio Anatomo Patológico, una histología confusa que dificulta la homogenización de este tumor respecto al resto de tumores del organismo.
HISTORIA
El cáncer de próstata fue descrito macroscópicamente por primera vez por el anatomista veneciano Nicolo Masa en el año de 1536, en el mismo año en que Vesalius en Padua dibujaba por primera vez la anatomía de la glándula prostática.


En el año 1786 Hunter realiza experimentos con animales machos demostrando que la castración evitaba o prevenía el crecimiento de la glándula prostática, un hecho sumamente crucial que retomaría en el año 1941 Charles Bretón Huggings para el tratamiento de cáncer de próstata Metastásico, un tratamiento que le supondría el ganar premio Nobel de Medicina.

Adams en Londres en el año de 1853 diagnosticaría por primera vez de manera histológica el cáncer de próstata
Hacia finales del año 1940 el cáncer de próstata era considerada una enfermedad extremadamente rara, sumamente agresiva y con pocos medios para su diagnóstico precoz. Cabe mencionar sin embargo, que hacia finales de los años 40 a 50, la expectativa media de vida de las personas rondaba los 50 años, de manera que desarrollar un cáncer de próstata era extremadamente y raro, y aquellas personas que lo padeciesen, tendrían cuadros clínicos dramáticos de progresión rápida y gran letalidad.
EPIDEMIOLOGIA
Esta gráfica tomada de www.globalcancermap.com, refleja la incidencia de todos los tipos del cáncer del mundo, de la que debemos destacar que la incidencia de cáncer es mucho mayor en países industrializados probablemente secundario al uso de políticas sanitarias mucho más agresivas respecto al screenig del cáncer.

Epidemiología – Sobrediagnóstico y sobretratamiento
Con la incorporación del antígeno prostático específico en los años 80 como parte del la detección del cáncer de próstata, este tumor aumento exponencialmente sus cifras a favor de un tumor en estadios de presentación precoz, potencialmente curable y con el transcurso de los años con una disminución de la mortalidad específica por cáncer.
Así manifiesto el cáncer de próstata se constituyó como el tumor sólido más frecuente para los adultos mayores -solo por debajo del cáncer de piel- siendo la tercera causa de muerte por cáncer en Europa y la segunda en nuestro medio.
Esta gráfica del www.globalcancermap.com, refleja la incidencia del Cáncer de Próstata en la que nuevamente observamos la tendencia respecto a una mayor incidencia en países industrializados, sin embargo, es importante considerar que en muchos países industrializados, la población adulta mayor es mucho más robusta y sería un parámetro importante a considerar en la presencia de esta incidencia

Centrados en Europa comentaremos que los países del Norte y del Oeste tienen una alta incidencia de cáncer de próstata y que en los países del Sur y del Este la incidencia esta en continuo aumento. Aún así, como hemos mencionado la mortalidad ha disminuido y esto se ve reflejado en que la supervivencia relativa a 5 años ha aumentado del 73,4 % en el período de 1999 a 2001 a 83,4 % en el período de 2005 a 2007. (EAU: Guías Clínicas)

La siguiente tabla es tomada de la publicación de 2014 de la SEOM (Sociedad Española de Oncología Médica – 2014) y gráfica la incidencia de todos los tipos de cáncer. La incidencia del cáncer de próstata en esta gráfica es totalmente extrapolable a 2018.
Podemos ver que la incidencia es del cáncer de próstata es muy alta, comparado solo con el cáncer de pulmón, más sin embargo, la mortalidad del cáncer de próstata es extremadamente baja lo que se ve reflejado una gran prevalencia de pacientes con cáncer de próstata. Comparativamente el cáncer de pulmón tiene también una incidencia alta pero su letalidad es mayor por lo que su prevalencia es mucho más baja que la del cáncer de próstata.
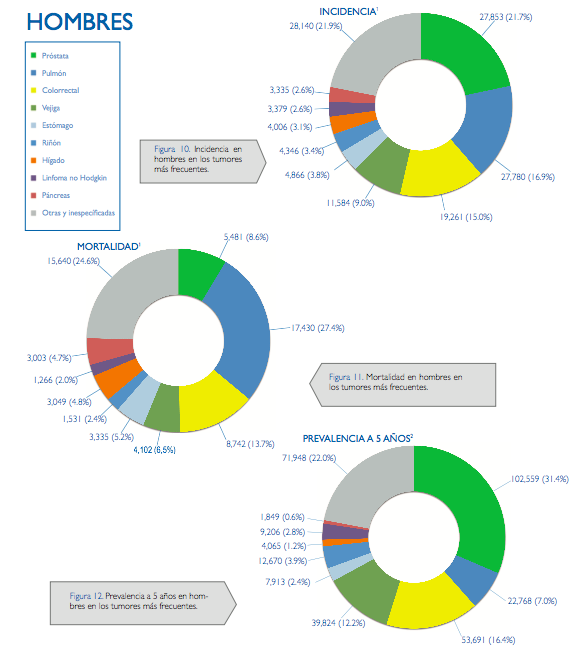
Cabe mencionar que la incidencia de cáncer de próstata se ha triplicado en los últimos 40 años. La disminución de la mortalidad del cáncer de próstata es probablemente expensas de un sobre diagnóstico y un sobre tratamiento de los pacientes (ESMO: Guías Clínicas del 2012). Como hemos mencionado, el Cáncer de Próstata se detecta en estadios precoces de enfermedad, además es un tumor que responde bastante bien a la terapia oncológica y su curso clínico suele ser en la mayoría de los casos lento.
Parece existir una predisposición genética relacionada al cáncer de próstata sustentado bajo grandes estudios epidemiológicos basados en factores Étnicos-Raciales e Historia Familiar. Veremos que los Japoneses y los Hindúes en sus zonas de origen tienen una baja incidencia de Cáncer de Próstata, mientras que los Africanos en sus zonas de origen tienen una incidencia alta, y los Afro Americanos tienen una incidencia de Cáncer de Próstata del doble con una presentación más frecuentemente en estadios avanzados. Existen estudios que demuestran que los japoneses que migran a latitudes con mayor incidencia de cáncer de próstata aumentan sus cifras a las del lugar de destino. (EAU: Guías Clínicas)
Un dato importante a mencionar dentro de la epidemiología del CaP es que la frecuencia del CaP Incidental y el de las Autopsias son similares globalmente, sin embargo como sabemos la incidencia clínica es diferente de país a país.
Estos hallazgos sugieren que existen factores exógenos como la dieta, el comportamiento sexual, la exposición a luz ultravioleta, la inflamación crónica o la exposición ocupacional las que podría condicionar un cambio desde un Cáncer Latente hasta el desarrollo de un Cáncer Clínico. (EAU: Guías Clínicas)
Con este razonamiento existieron estudios para intentar determinar factores protectores para el Cáncer de próstata sin embargo todos estos estudios han resultado negativos en las últimas décadas. Lo más significativos son los del Selenio, Vitamina E, licopenos y recientemente las estatinas siendo todos negativos. A día de hoy; no existen recomendaciones dietéticas para la prevención del Cáncer de Próstata.
Lo que si se ha encontrado es una correlación débil con el IGF – 1 y a Ingesta Alta de Proteínas y el incremento del Cáncer de Próstata. Respecto al Síndrome metabólico, aunque este no se asocia a un incremento de riesgo para desarrollar Cáncer de próstata., si que existe correlación con dos de sus componentes. Tanto la HTA como la circunferencia abdominal > 10 se asociaron a un incremento del Cáncer de Próstata de 15 al 56 % respectivamente, sin mediar ninguna repercusión bajo ninguna intervención relacionada a estos dos parámetros clínicos.
Un dato clave e importante a recordar como Urólogos, es que la Terapia Sustitutiva con Testosterona no aumenta el riesgo para desarrollar Cáncer de Próstata.
(EAU: Guías Clínicas)
| No existen recomendaciones dietéticas |
| Selenio / Vita E / Licopenos /Estatinas negativos |
| Existe una correlación débil con el IGF – 1 y la ingesta alta de proteínas e incremento del cáncer de próstata |
| Sd metabólico no se asocia a incremento de riesgo de CaP. |
| HTA y la circunferencia abdominal > 10 se asocio a incremento del Ca P |
| La terapia sustitutiva con Testosterona no aumenta el riesgo |
Cáncer de Próstata Hereditario
Hasta un 9% del Cáncer de Próstata tiene una presentación Familiar y constituye el Cáncer de Próstata Hereditario. El Cáncer de Próstata hereditario se define como aquel en el que se encuentran al menos tres o más familiares afectados o al menos dos familiares afectados con una presentación menor a los 55 años. Epidemiológicamente hablando, un familiar de primer grado duplica riesgo de cáncer próstata, mientras el tener más de dos familias de primer grado incrementa el riesgo de 5 a 11 veces. Aquellos pacientes en lo que se demuestra además la expresión del gen BRCA 2 presentaran tumores mucho más agresivos. La única diferencia que existe respecto a los casos índices, esporádicos, es que la presentación de estos casos suele ser de 6 a 7 años antes de la presentación habitual.
Existen más de 72 locis relacionados a la susceptibilidad para desarrollar cáncer de próstata y estos podrían explicar aproximadamente el 30% de riesgo familiar
(EAU: Guías Clínicas)
| Ca P Hereditario (9%) |
| Al menos 3 o más familiares afectados |
| Al menos 2 con presentación menor a los 55 años |
| 1 familiar de primer grado duplica el riesgo |
| Más de 2 de primer grado incrementa de 5 a 11 |
| BRCA2 más agresivo. |
| Se presenta unos 6 a 7 años antes con similares características |
EL NUEVO PARADIGMA
El Paradigma Diagnóstico Terapéutico del Cáncer de Próstata ha cambiado sustancialmente en los últimos 15 a 20 años, resultado de un conocimiento mucho más amplio de este tipo de tumor basado en un gran soporte en la evidencia clínica contemporánea.
A día de hoy, los Urólogos no pretendemos diagnosticar todos los tipos de Cáncer de Próstata. El diagnóstico del Cáncer de Próstata en nuestros días esta abocado al diagnóstico del Cáncer de Próstata Significativo o de Riesgo Alto, es decir que justificara un compromiso en la vida del paciente. En la medida de lo posible, se debe evitar el diagnóstico del Cáncer de próstata insignificante, de bajo de riesgo o indolente. Es más, en principio, debería excluirse de los programas de cribado oportunista a aquellos pacientes con una edad mayor a los 75 años o con expectativa de vida por debajo de los 10 a 15 años, o con comorbilidad importante o con un mal estatus funcional.
La siguiente tabla muestra las recomendaciones actuales para el screening del Cáncer de Próstata según las Guías de la EAU. Observe que el ítem final (*) esta en concordancia con la pretensión de un diagnóstico selectivo de pacientes de Alto Riesgo y que puedan beneficiarse de un tratamiento específico.
| Recomendaciones para screening CaP de la EAU
(European Association of Urology) |
| 1.- Hombres mayores de 50 años. |
| 2.- Hombres mayores de 45 años con antecedente familiar de CaP. |
| 3.- Origen Afro – Americano |
| 4.- PSA > 1 ng /ml en varones de 40 años |
| 5.- PSA > 2 ng /ml en varones de 60 años |
| * Todos los pacientes deben tener una expectativa de vida de por lo menos 10 a 15 años y un estado funcional bueno |
Por otro lado, el diagnóstico del cáncer de próstata en nuestros días, no implica necesariamente un tratamiento activo sobre nuestros pacientes y éste estará supeditado a parámetros clínicos del individuo como del propio tumor. Existen alternativas terapéuticas consideradas a día de hoy como un manejo aceptable en pacientes diagnosticados con tumores de muy bajo riesgo, o de bajo riesgo, con el sustento de que estos tumores tienen un comportamiento más lento y según evidencia científica solo un 3 % de estos individuos morirán por su tumor. Estos manejos clínicos incluyen: la Observación Expectante y la Vigilancia Activa.

Aún así, es indispensable que el Uro – Oncólogo, informe adecuadamente al paciente sobre las ventajas y las desventajas de estas medidas y de manera oportuna clasifique a los paciente en función a su edad, comorbilidad y estatus funcional para otorgar de manera consensuada otra alternativa terapéutica si existieran cambios clínicos durante el seguimiento.
Dr. Luis Fernando Susaníbar Napurí
Urología y Medicina Sexual
Madrid Urología
Fijo: 910 32 73 74






















